3D打印微针的无线智能创可贴用于慢性糖尿病治疗
时间:2020-03-05 10:13 来源:南极熊 作者:中国3D打印网 阅读:次
迄今为止,大多数研究都集中在寻找促进慢性伤口愈合所需的性能更优异的药物或确定药物释放的最佳时间曲线上。换言之,试图找到“用什么”和“何时”向伤口递送。但是慢性伤口是一种无血管或血管不充分的组织,被坏死组织和结痂覆盖。伤口的渗出液可以洗掉局部递送的治疗药物,或者由于存在各种酶而使它们失去活性。因此,Ali Tamayol团队的研究人员认为为了获得更好的治疗效果,在治疗有效性上应该阐明“何地”,即药物递送点的重要性,将药物直接送入活体组织,缩短治疗药物的传播距离。
近期,内布拉斯加州大学的Ali Tamayol团队发表在Advanced Functional Materials杂志上题为A Wirelessly Controlled Smart Bandage with 3D-Printed Miniaturized Needle Arrays的文章,提出了一种治疗慢性糖尿病伤口的个体化智能绷带(图1)。这种可穿戴、可远程控制的绷带配有生物相容性微针阵列(MNA),用于将多种重要的药物和生长因子绕过表层的结痂和坏死组织,直接输送到伤口床的深层。与局部给药相比,这种新方法在促进再上皮化和血管生成,促进伤口闭合和毛发生长方面更为有效。此外,由于MNA微针贴片具有微创性,诱发的疼痛和炎症也很小。
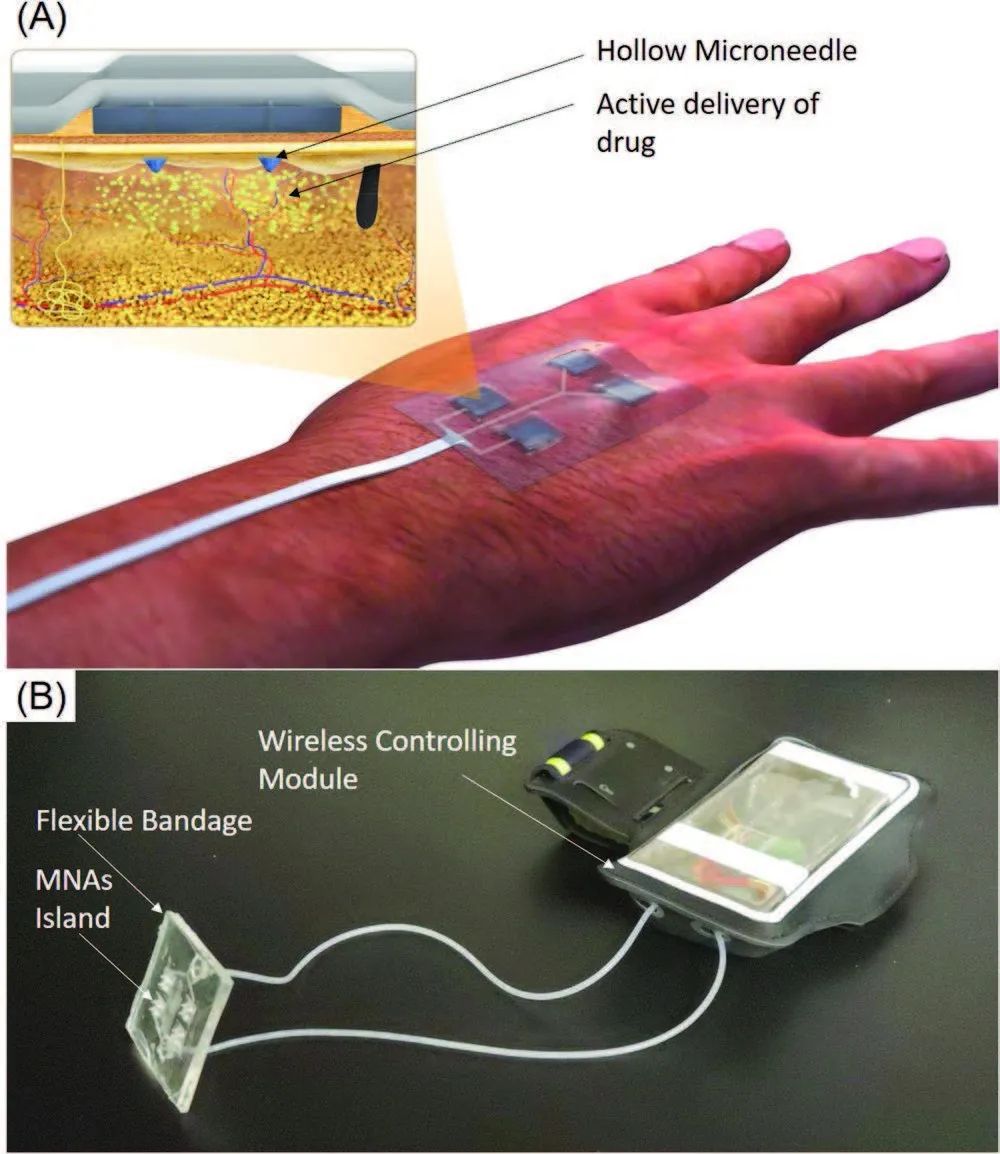
图1 无线控制的智能绷带,配有用于治疗的MNAs
基于以上想法,该智能绷带有2个模块组成,一个是由聚二甲基硅氧烷(PDMS)微通道层连接MNAs微针阵列贴片制成的一次性柔软绷带模块(图3A),另一个是可重复使用的控制模块,包含药物贮存器、微型泵、电源和电路(图3E),两者通过柔性硅管流道连接。
对于一次性绷带模块,研究人员首先使用熔融沉积(FDM)3D打印技术从生物相容性树脂中打印出设计的空心MNA微针结构,随后将其浸泡在NaOH溶液中去除支撑材料(图2A)。对于插入皮肤给药的微针而言,其中最主要的一个设计参数是MNA的长度。基于人类真皮和表皮的厚度,选择的微针长度为2mm。此外,为了保证绷带整体的柔韧性、透明可观察性,在厚度约为1.5mm的PDMS层上制备了微通道,然后将微通道的末端连接到多个面积为10 mm×10 mm的MNAs片上。
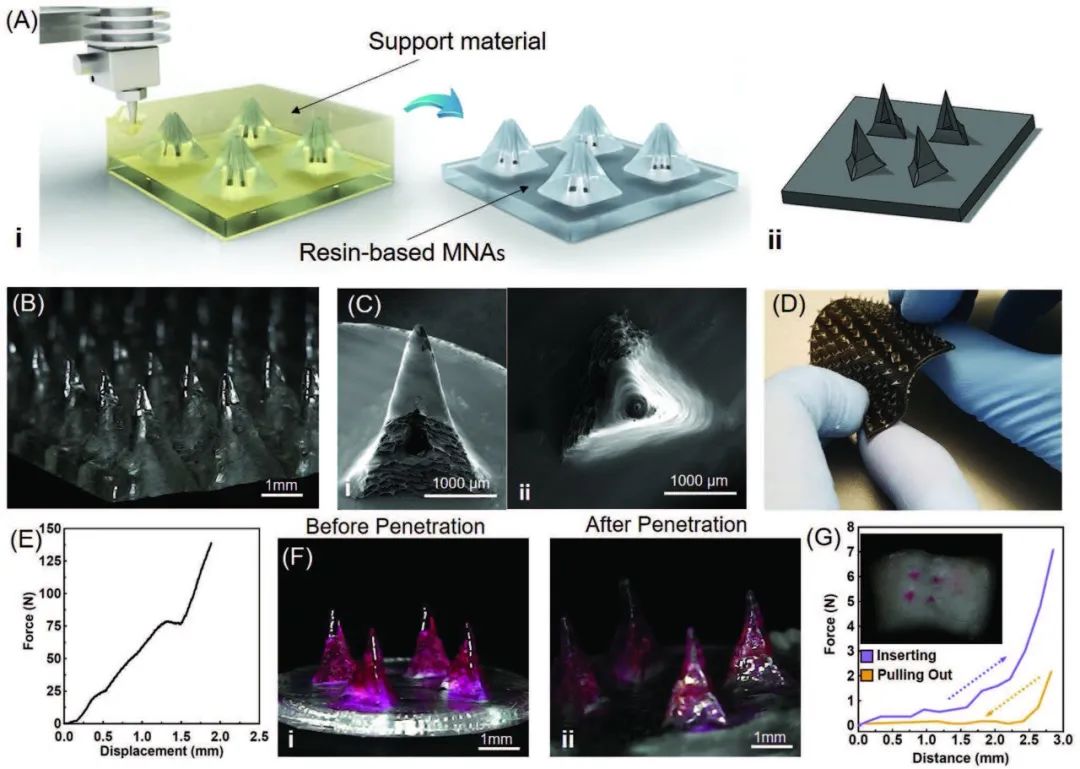
图2 3D打印MNAs的制备与表征
显然,该绷带模块能否使用还需要经过生物相容性和力学性能两方面的测试。研究员将血管内皮细胞(HUVECs)置于多孔培养板中,并将MNAs置于其培养基中。经过阳性对照实验表明树脂基MNAs并未对细胞增殖产生影响。对于力学测试,研究员进行了MNAs压载实验。如图2E所示,MNA没有断裂,仅在约78N的压缩力下弯曲。并且将其从猪皮上穿透和取出后,未观察到变形或破损(图2F)。大多数MNA以小于2N的力穿透新鲜猪皮,7N左右达到完全穿透,而拔出力为2N左右(图2G)。而MNAs与PDMS柔软基底层的连接强度通过剥离试验测定满足使用要求,其平均粘合强度为237KPa(图3B,C)。
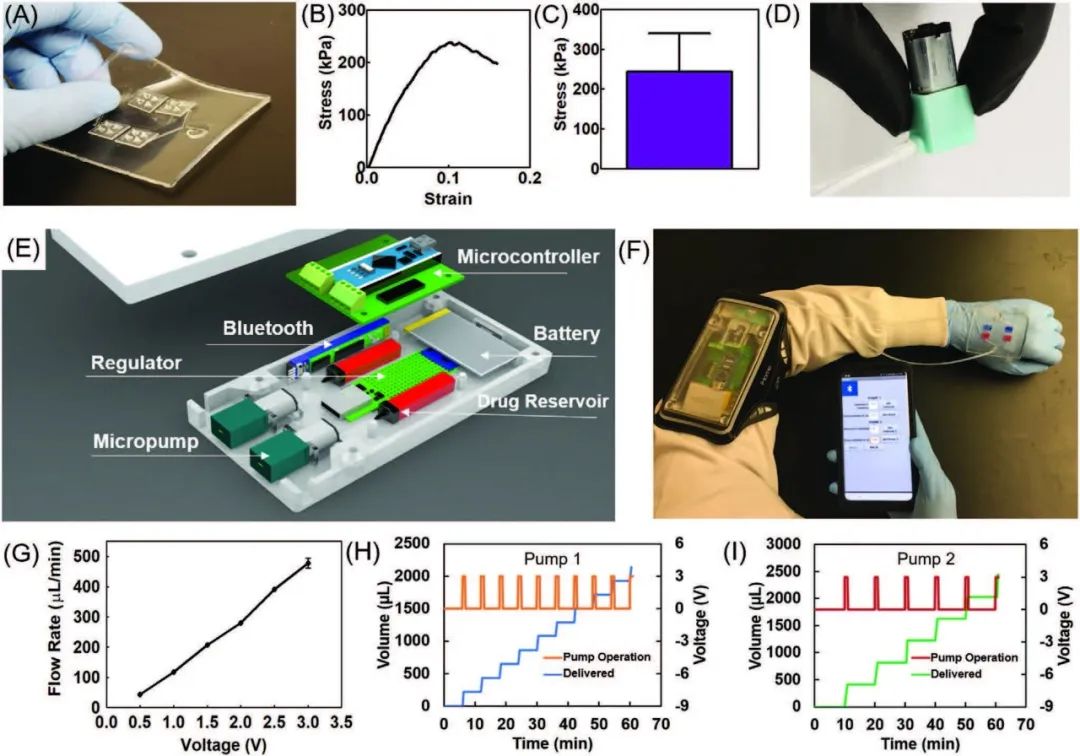
图3 微控制器和无线软件的特性
对于控制模块,使用蠕动微泵将药物溶液从贮存器经柔性硅管注入微通道阵列,然后通过各个MNAs贴片(图3F)。该模块可以通过蓝牙与智能手机上的对应APP连接进行远程控制,并标定流量-电压曲线实现精确控制(图3G-I)。为了防止药物在绷带中被潜在吸附。研究员使用牛血清白蛋白(BSA)和头孢唑林作为模型药物加载到绷带中,通过MNAs灌注后在不同时间点收集溶液,并使用总蛋白分析(BSA)和紫外可见分光光度法(头孢唑啉)测定药物浓度。实验结果表明蛋白质和抗生素的吸附量较低(图4A-B)。
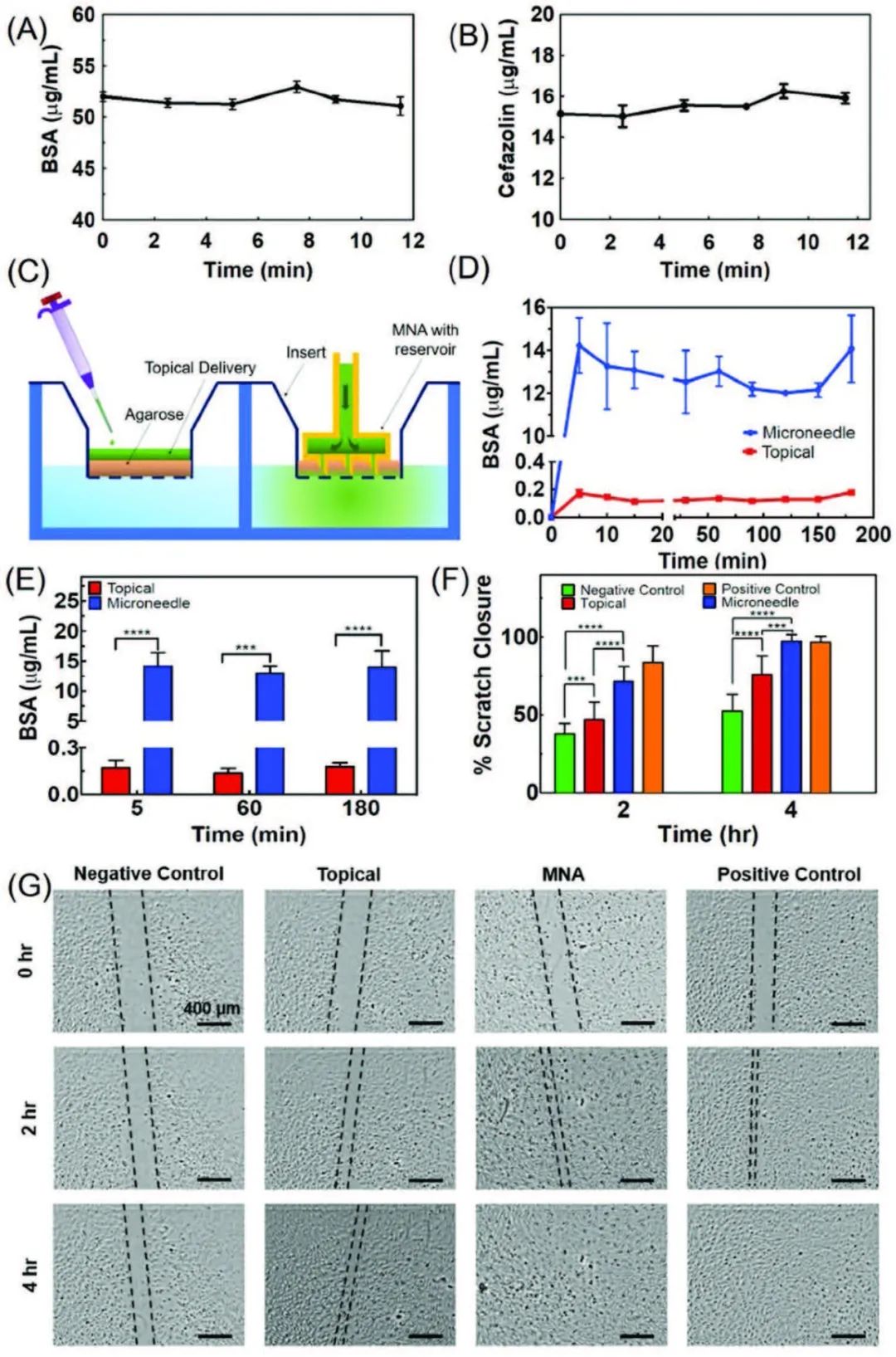
图4 药物释放特性及其对细胞培养的影响
为了评估MNAs在治疗慢性伤口中的重要性,研究员建立了一个模拟伤口组织的体外模型。体外模型由一个被2mm厚3%(w/v)琼脂糖凝胶包裹(提供与皮肤相似的孔隙率和质地)的细胞培养插入物组成(图4C)。为了模拟局部药物输送,在琼脂糖凝胶上添加100 μL药物溶液。为了测试基于MNAs的递送,通过3D打印制作了直径为10mm的微型绷带,并插入在琼脂糖凝胶中,然后使用注射器递送100微升药物溶液。体外模型结果表明,与局部传递的药物相比,MNAs能够将蛋白质快速传递到代表坏死组织环境的下腔室(图4D-E)。同理采用类似的方法,评价了血管内皮生长因子(VEGF)结合MNAs递送对于促进划痕愈合的积极作用(图4F-G)。
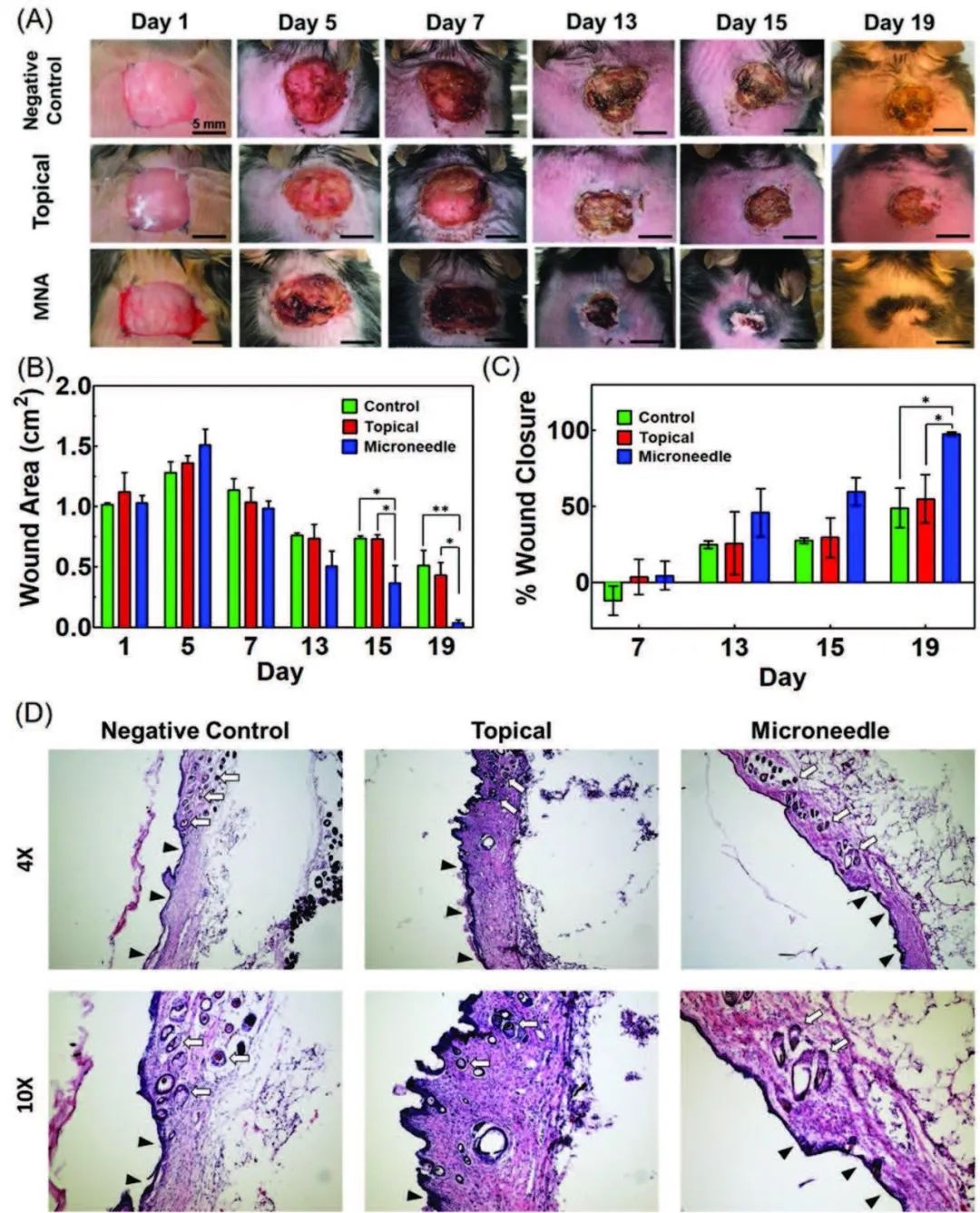
图5 VEGF经MNAs给药对糖尿病创面愈合影响的动物实验研究
最后,为了进一步研究MNAs在糖尿病和慢性创伤治疗中的潜在应用价值,研究员对糖尿病自发性突变小鼠皮肤创伤进行了动物实验。将动物分为三个研究组(图5A),包括:1)阴性对照,未治疗;2)局部用药,将VEGF溶液吸取到伤口上3)使用MNAs将VEGF溶液注入创面。根据动物实验结果,MNAs组相较与其他两组,平均伤口愈合率达到95%,肉芽组织厚度显著增加,并在新组织中观察到毛发生长以及作为血管化的标志CD-31大量表达(图5B-D)。虽然小鼠作为啮齿动物,无法完全匹配人类伤口愈合机制,但是得到的良好的实验结果可能应该在更相近的动物模型中也得到验证。
论文链接:
https://doi.org/10.1002/adfm.201905544
(责任编辑:admin)
最新内容
热点内容


 九天变三天!Fraunhofer基
九天变三天!Fraunhofer基 西北工业大学:基于氧空位
西北工业大学:基于氧空位 响应工业5.0,3D打印的450
响应工业5.0,3D打印的450 3DP4ME将在未来五年内交付
3DP4ME将在未来五年内交付 Pearson Lloyd采用可回收
Pearson Lloyd采用可回收 3D打印面料,可以帮助孩子
3D打印面料,可以帮助孩子 3D石墨烯泡沫制成
3D石墨烯泡沫制成 3D打印风力发电机
3D打印风力发电机 研究人员3D打印碳
研究人员3D打印碳 科学家受蜻蜓启发
科学家受蜻蜓启发 仅21小时3D打印!
仅21小时3D打印!

